近日,我院杨荣华/刘固寰教授团队成功开发了一种基于生物标志物响应的光催化体系,首次在活细胞内实现了生物-光双重调控的自由基聚合(PET-RAFT),成果发表于《J. Am. Chem. Soc.》,标题为:“Bio-Photo Dual Action of Intracellular Radical Polymerization”。该技术通过设计对活性氧/硫物种(ROS/RSS)和羧酸酯酶敏感的溴化荧光素(TBF)衍生物,利用“AND逻辑门”激活机制(需同时满足生物标志物触发与光照条件),解决了传统预合成聚合物递送效率低、脱靶泄漏及生物相容性差等核心瓶颈,为合成生物学提供了革命性工具。
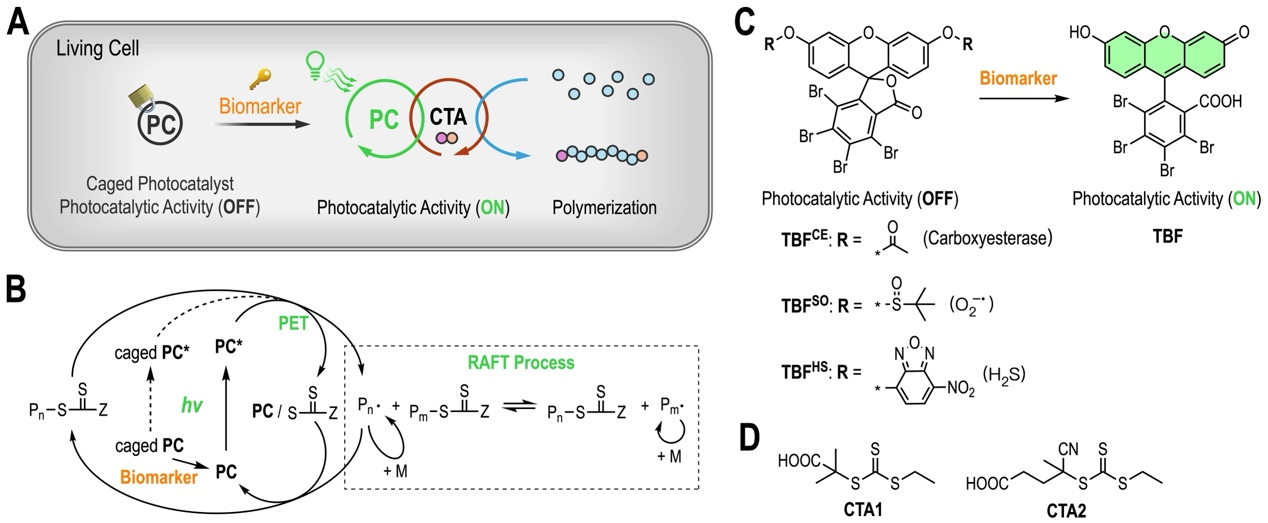
科学创新:研究团队通过仿生保护基团策略,使光催化活性严格受控于疾病微环境内源信号。实验证实,该体系能精准靶向特定细胞,并在内质网(ER)原位形成功能聚合物,通过破坏ER结构选择性诱导细胞死亡。相较于现有温度/pH/人工分析物触发方式,这一技术首次实现了与天然生物标志物的直接关联,其细胞相容性经体外/体内实验系统验证,为器官特异性治疗提供了新范式。
应用前景:此项研究不仅填补了双重刺激调控聚合在活体应用的技术空白,更开创了亚细胞器精准操控的化学方法论。研究者指出,该平台可灵活适配不同生物标志物,未来有望拓展至线粒体、溶酶体等细胞器功能调控,推动神经退行性疾病、肿瘤治疗等领域的突破性发展。
我院刘固寰教授为论文通讯作者,硕士研究生吴春晓和魏泽为论文共同第一作者,湖南师范大学为论文唯一通讯单位。本研究得到了国家自然科学基金项目、湖南省杰出青年科学基金等项目的支持。
全文连接:https://doi.org/10.1021/jacs.5c10871